Čarovné slovíčko, ktoré plní sny, neexistuje len v rozprávkach. Znie to ako zlato. V jadre je to obyčajný žltý kov, vďaka čomu dostal svoje meno. Otázka, ako získať zlato, zaujímala ľudí pred 7 000 rokmi, vo vzdialenej neolitickej ére. Práve vtedy si začal získavať neuveriteľnú popularitu vďaka svojej farbe spojenej so slnkom a silou danou bohmi. V súčasnosti si ho s nebesami spája málokto, no ako symbol moci a bohatstva zlato nielenže nestratilo svoj význam, ale stalo sa aj štandardom ekonomickej a s ním aj politickej nezávislosti všetkých krajín.
Zlato v prírode
Dôležité je vedieť nielen to, ako sa zlato ťaží, ale aj to, odkiaľ sa na našej planéte vzalo. Odpoveď na túto otázku pomáha pochopiť, kde hľadať tento vytúžený kov. Vedci naznačujú, že zlato vzniká pri výbuchu neutrónových hviezd, keď sa do vesmíru vrhajú tony prachu, ktorý obsahuje spolu s inými kovmi aj zlato. Následne sa prach koncentruje a vytvára hviezdne sústavy a planéty. Tak to bolo aj s našou Zemou. Teraz je väčšina zlata vo svojom roztavenom vnútri a „kvapka po kvapke“ sa vrhá na povrch lávou. Preto sa zlatonosné žily, kde sa dá zlato pomerne ľahko ťažiť, nachádzajú najmä v miestach postmagmatických a hydrotermálnych procesov. Ostatné vyvrelé horniny, ktoré sú ľahšie, sa časom vymyjú a zlato zostáva v sypačoch. To isté sa deje so zlatom, ktoré na Zem priniesli meteority. Môžeme ho nájsť v čistej forme (zlaté nugety), alebo v niektorých mineráloch, napríklad v sulfidoch, arzenidoch a 15 ďalších.
Vlastnosti zlata
Predtým, ako si povieme, ako zlato získať a z čoho, zoznámime sa s jeho vlastnosťami. Tieto poznatky pomôžu nestratiť pri ťažbe ani miligram drahého kovu. Aké sú teda vlastnosti zlata?
- Je veľmi hustá a ťažká. Zlatá guľa s priemerom len 5 cm váži celý kilogram! Táto vlastnosť sa využíva pri hlavnom spôsobe jeho extrakcie – praní.
- Je veľmi plastický, mäkký a v dôsledku toho tvárny. Zo zlata môžete vyrobiť nite hrubé ako ľudský vlas a priesvitné pláty tenšie ako papier. Vďaka tomu je možné ho použiť aj na SIM kartách!
- Môže sa topiť a vrieť, ale teploty musia byť dosť výrazné. Dôležité: v roztavenej forme, bez čakania na var, sa zlato môže rýchlo odparovať.
- Je nezvyčajne inertný, to znamená, že sa prakticky nerozpúšťa v kyselinách (iba v aqua regia av niekoľkých ďalších rozpúšťadlách).
Všetky tieto vlastnosti zlata sa využívajú pri spôsoboch jeho ťažby v prírode aj doma. 
Kde sa ťaží zlato
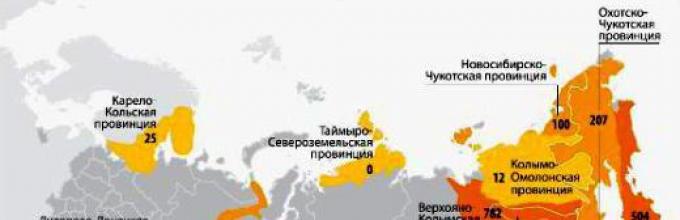
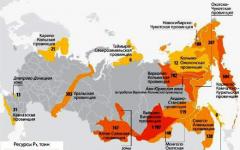
Na svete je niekoľko krajín, ktorým príroda nadelila ložiská zlata. Ide o Čínu (líder v ťažbe zlata), Austráliu, Rusko, Kanadu, Spojené štáty americké, Južnú Afriku, bývalý sovietsky Uzbekistan, Peru, Brazíliu, Mexiko, Čile, Indonéziu, Ghanu a Novú Guineu. Ťažba zlata sa vykonáva aj v iných krajinách, ale v príliš malom množstve. Naša krajina je na treťom mieste po Austrálii a Číne. Ruskí občania sa nepochybne zaujímajú o to, kde sa v Rusku ťaží zlato. Máme 37 spoločností zaoberajúcich sa touto činnosťou. Lídrom medzi nimi je Polyus Gold. Takmer 95% celkového objemu zlata sa nachádza na Ďalekom východe, v regiónoch Amur, Krasnojarsk, Magadan, Irkutsk, na Čukotke, na území Chabarovsk, v Jakutsku (Sakha), Burjatsku, Transbaikalii, v Čeľabinsku a Sverdlovsku. regiónoch. Zároveň sa maximálna produkcia vykonáva na území Krasnojarska a maximálna dynamika jej nárastu sa pozoruje v regiónoch Sverdlovsk a Magadan a na Chukotke. Ale v Transbaikalii sa zlato ťaží čoraz menej. Medzi bane a ložiská možno nazvať Dome, Kyuchussky, Maisky, Karalveemsky, Vorontsovsky, Eldorado, Diablov žľab, Sukhoi Log a ďalšie. 
Amalgamácia
Toto je jedna z najstarších a najnezdravších metód ťažby zlata, oficiálne zakázaná v Rusku, ale používaná v iných krajinách a našimi remeselnými ťažiarmi zlata. Spočíva v použití ortuti. Ako ťažiť zlato amalgamáciou? Na tento účel sa ortuť pridáva do plastovej alebo sklenenej misky obsahujúcej piesok a veľmi jemné frakcie zlata. Požadovaný kov nerozpustí, ale vtiahne do svojich guličiek. Aby ste pomohli procesu, musíte otočiť zásobník, aby sa ortuť prevalila po celom povrchu piesku. Ortuťové guľôčky so zlatom sa nazývajú amalgám. Zhromažďuje sa, oddeľuje od piesku a podrobí sa pôsobeniu buď kyselinou chlorovodíkovou, pri ktorej sa ortuť rozpustí, ale nie zlato, alebo odparením ortuti nad ohňom. Môžete to urobiť na jednoduchej panvici. V kyseline sa zlato zbavené ortuti usadzuje vo vločkách na dne, potom sa dôkladne premyje. Ak nie je túžba stratiť ortuť, musíte do kyseliny spustiť kúsok fólie. Táto jednoduchá technika umožňuje zrážanie ortuti. Z amalgámu je možné získať zlato jednoduchým filtrovaním cez semiš alebo plachtu, ale strata drahého kovu je vždy veľká. 
splachovanie
Ide o najstaršiu a ekologickejšiu metódu založenú na vysokej hustote zlata. Splachovanie sa používa ako v priemyselnej výrobe, tak aj v jednotlivých, v aluviálnych ložiskách. Spočíva v umývaní skál vodou. V tomto prípade sú všetky ľahké častice odstránené a ťažké, vrátane zlata, zostávajú na dne podnosu. Nevýhodou tejto metódy je, že príliš malé čiastočky zlata sa vymývajú vodou, čím sa výrazne znižuje jeho produkcia. Niektorých zaujíma, či môžu zlato ťažiť aj súkromné osoby. Áno môžeš. V Rusku bol prijatý zákon, ktorý umožňuje baníkom pracovať v malých ložiskách a utratených zlatých žilách. K tomu je potrebné zakúpiť si licenciu s platnosťou 5 rokov.
Kyanidácia
Táto najmenej pracovne náročná metóda je založená na rozpustení zlata v kyseline kyanovodíkovej. Ako ťažiť zlato kyanidáciou? Horninu, v ktorej je ušľachtilý kov, je potrebné rozdrviť, nasypať do vodotesnej vaničky, naliať kyselinu kyanovodíkovú, najmä kyanid sodný. Začne presakovať cez skalu a rozpúšťať zlato. Výsledný roztok sa naleje do samostatnej nádoby. Zlato v ňom obsiahnuté sa vyzráža napríklad zinkovým prachom a do procesu sa opäť vracia kyselina kyanovodíková. 
Flotácia
Tento spôsob nemožno nazvať ťažbou čistého zlata, no výrazne obohacuje horniny a uľahčuje ďalší proces. "Fleet", v preklade "flotter" - to je to, čo sa drží nad vodou. Ukazuje sa, že existujú skaly, ktoré sa dobre navlhčia a usadzujú sa na dne, a sú také, ktoré nezmáčajú, ale sú iba obalené tekutými časticami, ako sú vzduchové bubliny, a vďaka tomu „plávajú“ na povrchu. . Toto je flotácia. Pomocou neho sa zlato ťaží zo sulfidu, zlato-pyritu, zlata a medi a niektorých ďalších minerálov. Ruda sa rozdrví, naplní sa vodou a olejom (napríklad borovica), zmieša sa. Zlaté čiastočky plávajú na povrch. V priemysle namiesto oleja prechádza vzduch cez zmes vody a drvenej rudy a niektorých ďalších činidiel. Ďalšie čistenie zlata sa najčastejšie uskutočňuje kyanidáciou.
Ako ťažiť zlato doma
Metódy priemyselnej ťažby zlata sú, samozrejme, zaujímavé, ale pre väčšinu občanov nie sú príliš praktické. Nie každý si môže dovoliť ísť niekam na Sibír, do opustených baní. Áno, to nie je potrebné, pretože sa môžete stať prospektorom bez toho, aby ste opustili steny svojho vlastného bytu. Ako ťažiť zlato doma? Spôsobov je viacero. Najjednoduchšie a najpopulárnejšie od čias únie je získavanie drahého kovu z hodiniek a iných žltých produktov. Ukazuje sa, že skôr, s využitím inertnosti zlata, teda jeho antikoróznych vlastností, ním boli pokryté mnohé kovové predmety. Samozrejme, percento zlata v nich je malé, ale v horninách je tiež malé.
Takže ruda obsahujúca iba 5-10 gramov zlata na tonu sa považuje za bohatú. Čo treba urobiť s hodinami? Najprv ich nazbierajte čo najviac. Ďalej vezmite inertnú nádobu (sklo, plast), vložte tam hodinky, naplňte ich kyselinou dusičnou a počkajte, kým nerozpustí všetko okrem zlata. Výsledný roztok sa musí prefiltrovať cez niekoľko vrstiev gázy a na ňom uložené zlato by sa malo vložiť do vodky a nechať jeden deň stáť. Vznikne vám hnedastá zrazenina. Potom všetko dôkladne opláchnite vodou, znova prefiltrujte a nechajte roztopiť. Pre účinnosť tejto poslednej fázy sa do roztápajúceho sa zlata pridáva sóda. Je potrebné pamätať na to, že požadovaný kov sa môže odparovať, ale keď sa roztaví, prebytočné nečistoty ho opustia a sám sa zmení na malý ingot. 
Zlato z rádiových komponentov
Zlato sa používa v doskách plošných spojov a rádiových komponentoch kvôli svojej inertnosti a nízkej elektrickej vodivosti. Ako získať zlato z rádiových komponentov a mikroobvodov? Na to je vhodná aqua regia (zmes kyseliny dusičnej a chlorovodíkovej), ktorá sa pripravuje bezprostredne pred procesom. Táto pekelná zmes rozpúšťa zlato pri izbovej teplote. Existuje dokonca historický príklad rozpustenia zlatých medailí v aqua regia, aby ich ukryli pred nacistami. Proces produkuje chloraurátový ión, ku ktorému sa pridáva siričitan sodný. Zlato sa musí vyzrážať. Prefiltruje sa, premyje a roztaví na ingot.

Pred začatím procesu rozpúšťania je potrebné vytriediť zlatonosné časti od ostatných. Ďalej by ste sa mali pokúsiť čo najviac odstrániť všetko zbytočné zo „správnych“ rádiových komponentov. Osobitná pozornosť by sa mala venovať kovovým častiam, ako sú klobúky, nohy. Ak je to možné, mali by sa zbierať pomocou magnetu. Dosky je možné umiestniť do zmesi kyseliny chlorovodíkovej a peroxidu vodíka v pomere 2:1.
zlato z vody
Neuveriteľné, ale pravdivé: zlato je obsiahnuté v každej vode, z ktorej sa dá teoreticky aj extrahovať. V akej je koncentrácii? Ukazuje sa, že asi 5 kg na km štvorcový a v morskej vode je to niekoľkonásobne viac ako vo vode z vodovodu. Pomerne veľké množstvo zlata je aj v tavenine tečúcej z hôr a v sedimentoch bahna, najmä mineralizovaných. Predpokladá sa, že v tone bahna Červeného mora - asi 5 g zlata. Hlavný spôsob jeho extrakcie je nasledovný: pridať nehasené vápno do vody, odfiltrovať zrazeninu, vypustiť vodu späť do mora alebo rieky a sediment podrobiť ďalšiemu spracovaniu, napríklad kyanidácii.
virtuálne zlato
Pre všetkých hazardných ľudí, ktorým záleží na samotnom procese ťažby zlata, prišli informatici s hrou Minecraft, ktorej cieľom je stať sa úspešným baníkom po absolvovaní desiatok testov. Ako získať zlato v Minecrafte? Treba prejsť niekoľkými levelmi, „pracovať“ ako baník, premeniť vyťaženú rudu na ingoty a až potom z nej vyrobiť napríklad bojové brnenie. Požadovaný kov môžete hľadať aj v starobylých hradoch a kobkách, „spýtať sa okolo“ ľudí, ktorí sa stretávajú na náročných cestách prechádzajúcich levelov. Skutočným zlatokopom sa to zdá ako prázdna zábava, no hra Minecraft dobyla všetky kontinenty okrem Antarktídy a svojim vývojárom priniesla toľko peňazí, že by ich závidel každý baník.
Zlato vo vode nie je mýtus, ale realita, ktorá nevyžaduje potvrdenie. Ióny 79. prvku tabuľky D. I. Mendelejeva sú prítomné v ľudskom tele, sú súčasťou rastlín a samozrejme vody. Zvyčajná kvapalina je bohatá na drahý kov, nesie zlato, nesie jeho častice pozdĺž dna rieky a vytvára ložiská. Táto kvalita vody je zaujímavá pre baníkov po celom svete, ktorí nadšene skúmajú rieky a potoky.
Nájdenie zlata vo vode
Kde a ako hľadať Au?
Zlato sa ťaží z vody v zime aj v lete. Tento prvok možno nájsť niekoľkými spôsobmi a chladné počasie skúseného hľadača nezastaví. Na začiatok stojí za to preštudovať si algoritmus akcií, ktoré pomôžu extrahovať vzácny kov z vody.
Takže, čo robiť pre tých, ktorí chcú nájsť Au:
- Preskúmajte okolie, vyberte si miesto, porozprávajte sa trochu s miestnymi. Dodatočné informácie nebudú nikdy zbytočné, z tohto dôvodu sa oplatí dôkladne preštudovať oblasť, pozrieť si mapy a zozbierať čo najviac informácií. Rozhovor s miestnymi obyvateľmi pomôže zistiť, kde bolo Au nájdené, ako dávno to bolo.
- Obsah zlata vo vode môže príjemne prekvapiť a dokonca aj potešiť, ale aby ste ho našli, nemali by ste sa potápať pod vodu. Môžete jednoducho preskúmať skaly, preskúmať veľké kamene, odobrať vzorku vody.
- Pomocou podnosu musíte odobrať vzorku piesku alebo preskúmať breh rieky alebo potoka na prítomnosť kremenných kamienkov. Kremeň je hlavným spoločníkom zlata, no nielen ho môžete hľadať, Au môže „sprevádzať“ pyrit a striebro.
Ako získať zlato a aké zariadenia možno použiť pri ťažbe drahých kovov:
- Voda obsahuje zrnká piesku Au, ktoré však neplávajú prúdom, ale plazia sa po dne. V priebehu rokov sa zrnká piesku lisujú a môžu sa zmeniť na nugety a dokonca aj usadeniny. Mini-bagrovať pomôže odhaliť kov na dne. Ide o zariadenie, ktoré funguje ako vysávač. Mini bagr nasáva piesok a pomáha odhaliť Au. Samotný stroj filtruje, preplachuje a oddeľuje zlato od nečistôt a nečistôt.
- Detektor kovov je ďalším zariadením, ktoré pomáha odhaliť drahý kov v rieke alebo potoku. Zariadenie je ponorené do vody, dokáže reagovať na zlato a detegovať ložisko v malej hĺbke. Dokonca aj s pomocou detektora kovov preskúmajte pobrežnú zónu.
- Naši predkovia používali pri umývaní Au zásobníka. Spočiatku sa zariadenia vyrábali z koží oviec, neskôr sa technológia zmenila. Moderné podnosy sa používajú na prácu na horských riekach, rýchlo tečúcich potokoch. Pokrok však nestojí na mieste a napriek tomu, že moderné vaničky sú ľahšie a pohodlnejšie, používajú sa hlavne na odber vzoriek vody.
Prítomnosť nástrojov pomôže urýchliť vyhľadávanie a zvýši šance na úspech. To však vôbec neznamená, že drahé vybavenie je 100% zárukou detekcie nugetu v zemi alebo vo vode.
Zlato v piesku
Získavanie Au z pobrežného piesku začína tým, že sa odoberá na vzorku: jednoducho ho umyjú v podnose a skúmajú, či sú tam zrnká žltého kovu.
Môžete nakopať viac piesku, ponoriť ho do vriec a naliať do nich vodu. Faktom je, že piesok je oveľa ľahší ako zlato. Ušľachtilý kov sa okamžite usadí na dne a je ho vidieť, no zrnká piesku budú ďalej plávať vo vrecku.

Schéma možného umiestnenia zlata v nádrži
Voda s pieskom by mala byť filtrovaná, ak nie je po ruke nič, čo by sa dalo použiť ako filter, potom sa kvapalina jednoducho vypustí. Odíde s pieskom a Au zostane na dne vreca.
Vzácny kov sa ťaží z piesku výlučne v lete, v zime hľadači jednoducho prehľadávajú pobrežnú zónu, skúmajú kamene, ale piesok neumývajú.
Najčastejšie sa piesok jednoducho odoberá, zdvíha sa z dna rieky alebo sa vykopáva pri brehu. Vzorka pomáha určiť, či sa na vybranom mieste nachádza Au a koľko sa ho na tomto mieste nachádza. Ak sa vám podarí nájsť viac ako jedno alebo dve zrnká zlata, môžete pokračovať v hľadaní. Ak je množstvo žltého kovu zanedbateľné, hľadajúci idú na iné miesto.
V akej hĺbke možno nájsť nuget?
- Zlato s hmotnosťou nie viac ako jeden gram sa najčastejšie nachádza pod vrstvou piesku 10-13 cm, nie je také ťažké ho získať.
- Ak zvýšite pôdu o 15–30 cm, existuje šanca, že nájdete hrudku s hmotnosťou viac ako 1,5 gramu.
- Ak sa prekopete k zemi, ktorá ide hneď po piesku, nájdete celý kus drahého kovu s hmotnosťou viac ako 100 gramov.
Ťažba Au je však spojená s určitými ťažkosťami a neexistujú žiadne záruky, že „vykopávky“ skončia úspechom. Z tohto dôvodu sa odporúča pred začatím hľadania preštudovať oblasť a odobrať vzorky pôdy, piesku a vody.
Nájdenie zlata v morskej vode
Ťažba drahého kovu z morskej vody má určité ťažkosti. Hovorí sa, že ak vyťažíte všetko zlato z morí a oceánov, jeho hmotnosť bude veľmi slušná. Ale dnes neexistuje jediná účinná metóda, ktorá by pomohla extrahovať Au z vôd oceánov a morí. Existuje však nádej, že čoskoro budú vedci v tejto veci stále schopní uspieť.
Baktérie dokážu extrahovať zlato z morskej vody. Nie je to tak dávno, čo sa zistilo, že mikroorganizmy sú schopné odhaliť kovové častice, aj keď na bilión kubických metrov vody pripadá niekoľko zŕn Au.
Baktérie precipitujú kovové ióny a spájajú ich, čo si vyžaduje určitý čas pre mikroorganizmy.
Keďže táto metóda extrakcie je stále v procese výskumu, napriek všetkým vyhliadkam ju možno len ťažko nazvať efektívnou.
V zásade si odborníci v mnohých krajinách už dlho lámu hlavu nad tým, ako extrahovať Au z morskej vody. Existuje niekoľko metód, ale všetky sú považované za príliš drahé a z tohto dôvodu sa nepoužívajú v priemysle ťažby zlata.
Zisk a perspektíva
Bez ohľadu na to, kde sa Au ťaží, vo vode alebo na súši, priemysel ťažby zlata je teraz hodnotený ako perspektívny.
Objemy produkcie neustále rastú, geológovia hľadajú nové ložiská a technologický pokrok nezaháľa. Vynález rôznych druhov zariadení pomáha reštartovať rozvoj ložísk, ktoré boli predtým opustené a boli považované za neperspektívne.
Vzácny kov je ľudským očiam ukrytý vo vrstvách horniny, veľké množstvo je ho hlboko v útrobách zeme. Zlato sa dostáva na povrch len v miestach sopečnej činnosti. Z tohto dôvodu ľudstvo dlhé roky premýšľalo nielen o tom, ako ho extrahovať z útrob zeme, ale aj ako extrahovať vzácny kov z morskej vody.
Zároveň v priebehu rokov láska ľudí k žltému kovu neoslabla. Zlato priťahuje a fascinuje, ale nielen vonkajšia krása priťahuje baníkov a bankárov.
Drahý kov je výhodná investícia. Kurzy neustále rastú a v podmienkach hospodárskej krízy stabilita zlata mnohých láka.
Odvetvie sa nepochybne rozvíja a ťažba Au sa stáva výnosným biznisom. Metal vyhľadávajú nielen zamestnanci veľkých firiem, ale aj cestovatelia, prospektori a len obyčajní ľudia, ktorí chcú riešiť finančné problémy alebo sa trochu zabaviť.
Nezabudnite však, že hľadanie kovu na profesionálnej úrovni si vyžaduje materiálne investície. Je potrebné zaobstarať si vybavenie, dostať sa k informáciám a nájsť si čas venovať sa objavovaniu zlatých baní. Vyhľadanie a rozvoj vkladu trvá v priemere minimálne rok.
Napriek tomu, že v súčasnosti je známych najmenej 60 prvkov rozpustených v morskej vode, v priemyselnom meradle sa extrahujú iba štyri. Sú to sodík, chlór (obyčajná kuchynská soľ), horčík a niektoré jeho zlúčeniny, ako aj bróm. Niektoré zlúčeniny vápnika a draslíka sa ťažia ako vedľajšie produkty pri procese získavania kuchynskej soli alebo pri extrakcii horčíka. Zvyčajne sa tieto produkty získavajú buď ako výsledok extrakcie z morskej vody, alebo pri spracovaní rias, koncentráciou vápnika a draslíka. Treba však poznamenať, že priemyselná extrakcia týchto prvkov priamo z morskej vody ešte nie je zvládnutá. Uskutočnilo sa množstvo pokusov extrahovať ďalšie minerálne zlúčeniny z morskej vody, ale priemyselná ťažba bola neúspešná. Mnoho metód bolo patentovaných aj na extrakciu kuchynskej soli, horčíka a jeho zlúčenín, brómu, jódu, draslíka, síranu vápenatého, zlata a striebra z morskej vody (Baudin, 1916; Černík, 1926; Niccali, 1925; S. O. Petterson, 1928; Vienne , 1949).
Extrakcia soli
Systematická výroba soli z morskej vody sa začala v Číne oveľa skôr ako v roku 2200 pred Kristom. e. Po stáročia bolo mnoho národov závislých od mora ako zdroja soli (Armstrong a Miall, 1946). A teraz soľ, extrahovaná z morskej vody jednoduchým odparovaním slnečným žiarením, zaberá významný podiel na celkovej bilancii spotreby soli v krajinách ako Čína, India, Japonsko, Turecko a Filipíny. Ročne sa na svete vyprodukuje asi 6 miliónov ton soli. Výroba soli odparovaním z morskej vody si spravidla vyžaduje horúce podnebie so suchým vetrom. Okrem blízkosti mora a horúceho podnebia však musí byť splnených množstvo ďalších podmienok: nízka priepustnosť pôdy v odparovacích nádržiach, prítomnosť rozsiahlych nízko položených oblastí ležiacich pod hladinou mora alebo zaplavených morom. príliv a odliv, nízke zrážky počas mesiacov aktívneho vyparovania, absencia riediaceho účinku sladkých riečnych vôd a napokon v súvislosti s nízkymi nákladmi na výrobu soli – dostupnosť lacných vozidiel či blízkosť trhovísk.
Asi 5 % všetkej soli spotrebovanej Spojenými štátmi sa vyrába odparovaním, najmä v oblasti San Francisco Bay, kde sa tento rybolov začal už v roku 1852. Na obr. 5 ukazuje umelé odparovacie jazierka blízko južného konca Sanfranciského zálivu. Tu s celkovou rozlohou asi 80 m2. míľ „Leslie Salt Company“ vyťaží ročne približne 1,2 milióna ton soli. Podobné soľné panvy sa nachádzajú aj v horných tokoch zálivov Newport a San Diego v južnej Kalifornii; ich ročná produktivita je 100 tisíc ton (Emery, 1960). Vypúšťanie morskej vody do odparovacích bazénov v blízkosti Sanfranciského zálivu sa vykonáva v období vysokej vody cez stavidlá v priehrade, ktorá bazén uzatvára z mora. Morská voda tu starne, kým sa jej značná časť nevyparí a neusadia sa v nej obsiahnuté soli.

Ryža. 6. Na odstránenie vrchnej vrstvy vykryštalizovanej soli sa používajú mechanické škrabky. V čase, keď dôjde k "zberu soli", je hrúbka vrstvy soli zvyčajne 4-6 palcov.
Síran vápenatý kryštalizuje z roztoku ako jeden z prvých. Po uložení solí síranu vápenatého na dno sa zvyšná soľanka opatrne prenesie do záhradného bazéna, kde v dôsledku vyparovania roztok ďalej hustne, až sa začne zrážať chlorid sodný. Odparovanie soľanky pokračuje, kým nedosiahne špecifickú hmotnosť asi 1,28, to znamená až do začiatku plnenia horčíkových solí. V tomto štádiu sa soľanka nazýva horká materská soľanka. Soľanka sa odoberá z klietkového bazéna a prepravuje sa do iných podnikov, kde sa z nej získavajú rôzne zlúčeniny horčíka, bróm a iné soli. Po odstránení soľanky sa do bazéna klietok opäť naleje čerstvá soľanka a celý cyklus získavania chloridu sodného sa opakuje. Do 1. augusta sa na dne takýchto bazénov nahromadí vrstva chloridu sodného s hrúbkou 4-6 palcov. Soľ sa odoberá pomocou mechanických škrabiek a nakladačov (obr. 6); potom sa soľ zmýva od rôznych nečistôt morskou vodou a ukladá sa vo forme veľkých kužeľovitých kôp (obr. 7). Soľ na priemyselné využitie sa vo väčšine prípadov ďalej nerafinuje. Dodatočne sa však čistí, ak je určený na konzumáciu potravín obyvateľstvom. Obsah NaCl v rafinovanom produkte presahuje 99,9 %. Náklady na soľ získanú voľným odparovaním morskej vody pod vplyvom slnka sa v USA pohybujú od 10 USD za 1 tonu surového produktu v blízkosti miesta ťažby do 150 USD za 1 tonu prečistenej a balenej kuchynskej soli.

Schéma získavania soli z morskej vody je na celom svete približne rovnaká, v mnohých krajinách však lacná pracovná sila umožňuje tento proces modifikovať.
V krajinách s odlišnou klímou, ako je Švédsko a Sovietsky zväz, sa soľ získava zmrazením morskej vody. Soľný ľad, ktorý pozostáva z takmer čistej vody, sa odfiltruje zo zvyškovej soľanky, na ktorej sa potom vykoná séria po sebe nasledujúcich operácií zmrazovania predtým, ako sa koncentrácia jeho zvyškových častí stane dostatočne vysokou na to, aby sa začalo odparovanie do sucha pôsobením umelých kúrenie (Armstrong, Miall, 1946) .
Koncentrovaná soľanka, ktorá zostane po oddelení chloridu sodného, sa podrobí ďalšiemu špeciálnemu spracovaniu, aby sa extrahovali zlúčeniny v nich prítomné. Pridanie chloridu vápenatého do roztoku teda spôsobí tuhnutie síranu vápenatého (sadry), ktorý sa potom predáva. Pri ďalšom zahustení soľanky sa vyzrážajú sírany horčíka, draslíka a iné soli. V záverečných fázach procesu sa zo zvyškového roztoku získa chlorid horečnatý a bróm.
Extrakcia brómu z morskej vody
Bróm možno považovať takmer za morský prvok, keďže 99 % celkového obsahu brómu v zemskej kôre je v oceáne (pozri tabuľku 2). Bróm objavil v roku 1825 francúzsky bádateľ A. J. Balard v koncentrovaných roztokoch získaných po vyzrážaní soli z vody slanísk pri Montpellier. Nedávno bol bróm nájdený v potašových ložiskách v Strasfurte a v soľankách z vrtov v Michigane, Ohiu a Západnej Virgínii. Bróm bol prvýkrát izolovaný z morskej vody v roku 1926 v Kalifornii pri úprave materských soľaniek získaných pri extrakcii soli v umelých odparovacích jazierkach. Spotreba brómu v priemysle bola pred výrobou vysokokompresných spaľovacích motorov relatívne obmedzená, takže dopyt na trhu uspokojili množstvá, ktoré sa ťažili z vrtov a soľných ložísk. Potom sa však situácia dramaticky zmenila. Etyléndibromid sa pridával do antidetonačného benzínu obsahujúceho aditívum tetraetyl olova, aby sa zabránilo usadzovaniu olova na stenách valcov, ventiloch, piestoch a zapaľovacích sviečkach. Pri takto zvýšenom dopyte po bróme sa soľanky čerpané z vrtov ukázali ako nedostatočné. Neuspokojil dopyt a ťažba brómu ako vedľajšieho produktu pri výrobe soli. Existovala naliehavá potreba iného zdroja brómu.
Pri rozsiahlom hľadaní ďalších zdrojov brómu vyvinula spoločnosť Ethyl Corporation proces priameho vyzrážania brómu priamo z morskej vody, ktorá nebola vopred koncentrovaná. Podľa tejto schémy sa bróm zráža vo forme nerozpustnej zlúčeniny - tribrómanilínu, keď sa morská voda spracováva anilínom a chlórom. Aby sa zabránilo hydrolýze chlóru, morská voda sa najskôr okyslí kyselinou sírovou. Neskôr sa tento proces rozšíril do rozsahu priemyselnej výroby. Jednotka bola inštalovaná na lodi, ktorá bola následne premenená na zariadenie na získavanie brómu. Takéto plávajúce zariadenie, ktoré funguje 25 dní v mesiaci, vyprodukuje asi 75 000 libier brómu. Za rovnaké obdobie závod spotrebuje reagencie: 250 ton koncentrovanej kyseliny sírovej, 25 ton anilínu, 66 ton chlóru, uložených medzi hornou a dolnou palubou. Účinnosť extrakcie brómu z morskej vody, kde ho obsahuje len 0,1 libry na 1 tonu, je asi 70 %. Loď má zavedené ochranné opatrenia, aby sa zabránilo zriedeniu morskej vody odpadovou vodou vypustenou po dokončení procesu. Neskôr sa zistilo, že pobrežné morské prúdy, ktoré existujú pozdĺž mnohých pobreží, možno úspešne využiť na zabránenie miešania. V súčasnosti sa verí, že z technického hľadiska bol proces extrakcie brómu na palube plávajúceho zariadenia úspešne vyriešený, ale práca na otvorenom mori s vysoko korozívnymi činidlami je oveľa náročnejšia ako na súši.
Výber miesta na výstavbu zariadenia na regeneráciu brómu by sa mal robiť veľmi opatrne. Zároveň je potrebné vopred vylúčiť možnosť riedenia morskej vody spotrebovanej zariadením zrážkami, splaškov, ako aj vodou, z ktorej už bol bróm extrahovaný. Okrem toho by morská voda mala mať vysokú a stálu slanosť, relatívne vysokú teplotu a nemala by byť znečistená organickým odpadom, ktorý plytvá chlórom. Takéto miesto, ktoré spĺňa všetky vyššie uvedené požiadavky, sa našlo neďaleko Cure Beach (Severná Karolína). Tu „Ethyl Dow Chemical Company“ postavila závod s kapacitou 3 tisíc ton brómu ročne. V roku 1938 sa kapacita tohto podniku zvýšila na 20 tisíc ton brómu ročne (Shigley, 1951).
Ďalší závod tohto typu je vybudovaný pri Freeporte, kde sú podmienky na extrakciu brómu z morskej vody vhodnejšie pre všetky technologické požiadavky ako pri Cure Beach. Projektovaná kapacita tohto závodu je 15 tisíc ton brómu ročne. V roku 1943 tam postavili ďalší závod rovnakej kapacity. Podnik neďaleko Cure Beach bol zatvorený na konci druhej svetovej vojny. Závody vo Freeporte teda v súčasnosti produkujú asi 80 % ročnej spotreby brómu v Spojených štátoch. Na obr. 8 je diagram procesu regenerácie brómu pre Ethyl Dow Chemical Company.

V továrni na Cure Beach bola podľa predtým vyvinutej techniky naliata zmes morskej vody, kyseliny a chlóru na vrchol tehlovej veže s drevenými mriežkami zabudovanými do nej. Bróm rozpustený v morskej vode bol redukovaný chlórom na relatívne prchavý elementárny bróm a kyselina prítomná v zmesi bránila hydrolýze chlóru. Keď zmes brómu a morskej vody odtekala z hornej časti veže, vzduch bol vyfukovaný zdola nahor. Prechádzajúci vzduch vynášal voľný bróm z morskej vody a transportoval ho do absorpčnej veže naplnenej uhličitanom sodným, po ktorej bola morská voda, ktorá už neobsahovala bróm, odvedená späť do mora. Na roztok sódy nasýtený brómom sa pôsobí kyselinou sírovou, aby sa bromičnany a bromidy sodné premenili na voľný bróm. Potom sa zmes prečerpala do odparovacej kolóny, kde sa oddestiloval bróm a znovu kondenzoval do sklenených alebo keramických nádob. Ďalšie čistenie brómu destiláciou umožnilo v konečnom dôsledku získať produkt s obsahom brómu až 99,7 %.
V roku 1937 bol tento proces trochu upravený. Pri primárnej destilácii brómu sa teda ako nosiče použili oxid siričitý a vzduch. V dôsledku toho sa uvoľnil bróm vo forme kyseliny bromovodíkovej, čo umožnilo výrazne zlepšiť jeho následné čistenie. Hoci oba procesy sú viac ako 90% účinné pri získavaní brómu, proces priamej extrakcie brómu z morskej vody pomocou oxidu siričitého sa v súčasnosti takmer výlučne používa v Spojených štátoch (Shigley, 1951).
Extrakcia horčíka z morskej vody
Horčík je najľahší z kovov používaných v stavebníctve. Jeho špecifická hmotnosť je 1,74, zatiaľ čo pre hliník je to 2,70 a pre železo je to 7,87. Tento kov sa najviac používa pri konštrukcii vozidiel. Okrem toho sa horčík používa ako zložka zliatin s hliníkom, v systémoch anodických a katódových ochranných povlakov, v zábleskových fotolampach a v mnohých ďalších oblastiach techniky. Do roku 1964 bola ročná svetová produkcia horčíka asi 150 tisíc ton.
Morská voda obsahuje približne 0,13 % horčíka. A napriek tomu, že táto koncentrácia je len 1/300 množstva nájdeného v horčíkovej rude ťaženej na súši, morská voda je pre Spojené štáty hlavným zdrojom tohto kovu. Horčík bol prvýkrát získaný z morskej vody v Anglicku (Armstrong, Miall, 1946), ale prvý veľký podnik na extrakciu horčíka z morskej vody postavila začiatkom roku 1941 blízko Freeportu spoločnosť Ethyl Dow Chemical Company. Dovtedy sa horčík v Spojených štátoch získaval z vrtov a ložísk magnezitu.

Výber miesta na výstavbu závodu pri Freeporte bol diktovaný nasledujúcimi veľmi priaznivými okolnosťami. Dostupnosť lacného zemného plynu umožňuje jeho efektívne využitie na výrobu tepla a elektriny. Geografická poloha závodu umožňuje odvádzať odpadové vody späť do Mexického zálivu s mimoriadne zanedbateľnou možnosťou riedenia spotrebovanej morskej vody. Veľmi lacné vápno sa dá získať z vápencových škrupín vyťažených zo dna Mexického zálivu, len pár kilometrov od továrne na horčík. Na obr. Obrázok 9 ukazuje vývojový diagram procesu na extrakciu horčíka v závode blízko Freeportu a jedna z častí tohto závodu je znázornená na obr. 10.

Ryža. 10. Celkový pohľad na závod na spracovanie horčíka v Ethyl Dow Chemical Company, Freeport (Texac). V popredí sú viditeľné zahusťovadlá Dorr, do ktorých sa čerpá zmes morskej vody a vápna, aby sa urýchlilo vyzrážanie chloridu horečnatého.
Morská voda vstupuje do elektrárne rýchlosťou asi 1 milión galónov za hodinu cez podvodné zámkové brány kanála spojeného s Mexickým zálivom. Výhodou takéhoto zásobovacieho systému je, že spodné vrstvy vody majú oveľa vyššiu slanosť ako povrchová voda v oblasti závodu. V umelom bazéne sa voda priebežne upravuje vápenným mliekom (vyššie bolo spomenuté, že vápno sa získava kalcinovaním lastúr ustríc). V dôsledku reakcie vápenného mlieka so zlúčeninami horčíka vzniká tekutá kalovitá zrazenina nerozpustného hydroxidu horečnatého, ktorá sa potom prečerpáva do usadzovacích nádrží. Sediment tvorí približne 2 % z celkového objemu morskej vody spotrebovanej pri tejto výrobe, inými slovami, už v prvej fáze technologického procesu sa uskutočňuje 100-násobná koncentrácia úžitkovej zložky. Odpadové vody klesajú do rieky Brasos, ktorá sa v značnej vzdialenosti od závodu vlieva do Mexického zálivu.
Prefiltrovaný hydroxid horečnatý sa rozpustí v kyseline chlorovodíkovej. Výsledný roztok chloridu horečnatého sa zahustí odparovaním, aby sa čiastočne zbavil solí zachytených z morskej vody. Vápnik sa vyzráža ako nerozpustný síran alebo sadra pridaním síranu horečnatého do roztoku, potom sa roztok opäť prefiltruje, aby sa oddelila sadra a iné soli, a potom sa zahustí odparením. Keď koncentrácia chloridu horečnatého dosiahne približne 50 % a teplota roztoku stúpne na približne 170 °C, nastrieka sa na predtým vysušený pevný MgCl2. Rozpúšťadlo sa okamžite zmení na paru a vyzráža sa chlorid horečnatý. Vysušená pevná zrazenina sa potom umiestni do elektrolytickej komory, kde sa rozkladá na kovový horčík a plynný chlór. Chlór sa premieňa na kyselinu chlorovodíkovú, ktorá sa úspešne používa v ďalších cykloch procesu. Kovový horčík sa vyberá z elektrolytickej komory a formuje sa do ingotov. Obsah kovov v nich presahuje 99,8 % (Shigley, 1951).
Celkový dopyt USA po surovom, primárnom kovovom horčíku sa od konca druhej svetovej vojny uspokojuje jeho výrobou z morskej vody. Počas vojny vláda USA vybudovala množstvo závodov, ktoré ako suroviny na výrobu horčíka využívali magnezit, dolomit, čerpanú soľanku a morskú vodu. Do konca vojny však žiadna z týchto elektrární nemohla konkurovať podnikom extrahujúcim horčík z morskej vody, a to aj napriek tomu, že vláda zaručila prvým závodom plný predaj produktov, zatiaľ čo podniky pôsobiace na morskej vode takéto nemali. záruky..
Voľba miesta na výstavbu horčíkovej elektrárne je daná menej prísnymi požiadavkami ako pri prevádzke, ktorá prijíma bróm z morskej vody. Výnimkou je však prípad, keď sa bróm a horčík extrahujú spoločne. V procese extrakcie horčíka teda teplota morskej vody nemá veľký význam a spotreba surovín je menej dôležitá: na výrobu 1 libry elementárneho horčíka sa spotrebuje iba 5 % množstva morskej vody, používa sa pri extrakcii brómu. Najdôležitejšími faktormi, ktoré určujú vhodnosť výberu miesta pre závod, sú blízkosť zdrojov lacného vápna, paliva a elektriny. Účinnosť procesu extrakcie horčíka z morskej vody je 85-90%. A hoci moderné technologické možnosti umožňujú oveľa kompletnejšiu extrakciu horčíka z morskej vody, nie je to ekonomicky realizovateľné, pretože sa odhaduje, že zvýšenie koeficientu obnovy o viac ako 90 % je sprevádzané prudkým nárastom kapitálových nákladov na každé percento. zvýšiť.
Jednou z podstatných výhod tohto procesu je, že nízke náklady na suroviny možno ďalej znížiť, ak sa tieto materiály privádzajú priamo do výrobnej linky ich čerpaním. Takéto mechanizované zásobovanie umožňuje do značnej miery kontinuálny výrobný proces a inštalovať automatické riadiace zariadenia. Okrem toho je pozitívnou vlastnosťou rastliny tohto typu extrémna rovnomernosť surovín, ktoré spotrebúva.
zlúčeniny horčíka
Horčík vo forme MgO, Mg(OH)2 a MgCl2 je široko používaný v širokej škále priemyselných odvetví. Používa sa ako žiaruvzdorný materiál pre vnútorné nátery v taviacich peciach, ako surovina pre farmaceutickú výrobu, v izolátoroch, pri výrobe hnojív, umelého hodvábu a papiera a mnoho ďalších. Mnoho spoločností vo svete získava zlúčeniny horčíka z morskej vody; je to typické najmä pre Anglicko a USA. Po prvýkrát sa priemyselná extrakcia zlúčenín horčíka z morskej vody uskutočnila ako vedľajší proces zo zvyškových soľaniek pri výrobe kuchynskej soli (Seaton, 1931; Manning 1936, 1938).

Ryža. 11. Postupnosť procesu v horčíkovom závode spoločnosti "Kaiser Aluminium Eid Chemical" neďaleko Moss Landing (Kalifornia).
Schéma procesu extrakcie zlúčenín horčíka z morskej vody je znázornená na obr. 11. Takáto technologická schéma sa používa v ich podnikoch Kaiser Aluminium and Chemical Corporation v blízkosti Moss Landing (Kalifornia). Morská voda sa mieša s kalcinovaným dolomitom. Vyzráža sa hydroxid horečnatý, ktorý sa potom usadzuje vo veľkých koncentračných nádržiach. Po usadení sa hydroxid horečnatý izoluje, premyje, aby sa odstránili rozpustné nečistoty, a prefiltruje, aby sa obsah vody znížil na približne 50 %. Časť takto získaného hydroxidu horečnatého sa predáva ako homogenizovaný filtračný koláč vo forme brikiet. Tieto produkty sa používajú pri výrobe papierových a magnéziových izolácií. Časť zrazeniny, ktorá zostala na filtri, sa potom znovu kalcinuje za vzniku MgO rôznych stupňov, ktoré možno použiť pri výrobe umelého hodvábu, gumy, izolačných náterov, žiaruvzdorných tehál. Na obr. 12 znázorňuje závod Kaiser na výrobu zlúčenín horčíka.

Ryža. 12. Závod na extrakciu horčíka z morskej vodárenskej spoločnosti „Kaiser Aluminium End Chemical“ neďaleko Moss Leiding (Kalifornia) (foto z lietadla).
V USA sa asi 90 % celkového objemu žieravého kalcinovaného oxidu horečnatého a asi 50 % žiaruvzdornej magnézie získava z morskej vody alebo zo soľanky čerpanej zo studní.
zlato z morskej vody
Na vývoj metód získavania zlata z morskej vody sa vynaložilo toľko úsilia a peňazí, že v tomto smere je ťažké s ňou porovnávať akýkoľvek iný prvok. Na otázky súvisiace s ťažbou zlata z morskej vody bolo vydaných mnoho patentov, a to z hľadiska metód aj vybavenia (Bardt, 1927; Baudin, 1916; Bauer, 1912; Černík, 1926; Bitter, 1938; Stoces, 1925). V roku 1866 objavil jeden z členov Francúzskej akadémie vied prítomnosť stopového množstva zlata v morskej vode. A neskôr, v roku 1886, bolo oznámené, že obsah zlata vo vodách Lamanšského prielivu je až 65 mg na 1 tonu vody.
Na začiatku tohto storočia Svante Arrhenius poukázal na to, že predchádzajúce stanovenia obsahu zlata v morskej vode boli zveličené najmenej 10-krát. Výpočty samotného Arrhenia však ukázali, že minimálny obsah zlata v morskej vode nie je nižší ako 6 mg na 1 tonu.Podľa týchto výpočtov sa vo svetovom oceáne nachádza približne 8 miliárd ton zlata. Toto množstvo zlata stačí na to, aby sa každý človek na zemi stal milionárom. Ale napriek mnohým patentom a projektom sa z morskej vody ešte nezískali prakticky hmatateľné množstvá tohto kovu.
Na konci prvej svetovej vojny brilantný nemecký chemik a nositeľ Nobelovej ceny Dr. Fritz Haber tvrdil, že vojnový dlh Nemecka možno zaplatiť zlatom získaným z mora. Za predpokladu, že koncentrácia zlata je 5-10 mg na 1 tonu morskej vody, Haber obsadil výskumné plavidlo s príslušným personálom a vybavením na štúdium najvyššieho obsahu zlata v oceánoch. Haber však na svoju veľkú ľútosť zistil, že koncentrácie zlata zriedka prekračujú 0,001 mg na 1 tonu vody (Haber, 1927). Najvyšší obsah zlata je zaznamenaný v južnom Atlantiku a je 0,044 mg na 1 tonu.Ani v Sanfranciskom zálive, kde tečú rieky odvodňujúce zlatonosné oblasti, koncentrácia zlata veľmi neprevyšuje priemerný obsah tohto prvku v r. otvorený oceán. Po 10 rokoch práce na tomto probléme prišiel Haber k záveru, že ťažba zlata z morskej vody nie je rentabilná. Teraz sa zistilo, že Haberove hodnoty zlata v morskej vode sú trochu nepresné, pretože zjavne nezohľadnil prítomnosť zlata v chemikáliách a v reakčných nádobách, ktoré používal počas svojich analýz.
Metódy získavania zlata z morskej vody sú založené na použití sulfidových častíc, ktoré majú vysokú afinitu k zlatu. Keď morská voda prechádza cez tieto častice, predpokladá sa, že zlato priľne k povrchu sulfidov. Okrem toho bola ortuť tiež navrhnutá ako materiál na extrakciu zlata z morskej vody.
Napriek mnohým pokusom získať zlato z morskej vody je známy len jeden prípad, kedy sa podarilo získať nejaké hmatateľné množstvá tohto kovu. V súvislosti s rozsiahlymi prácami v závode na získavanie brómu v Severnej Karolíne skúmala spoločnosť Ethyl Dow Chemical Company ťažbu ďalších kovov vrátane zlata. V dôsledku spracovania 15 ton morskej vody sa podarilo vyťažiť 0,09 mg zlata, ktorého hodnota je približne 0,0001 USD. Dnes je toto zanedbateľné množstvo všetko zlato, ktoré bolo vyťažené z morskej vody (Terry, 1964 ).
Ostatné látky extrahované z morskej vody
Okrem bežnej soli, brómu, horčíka a jeho zlúčenín sa niekedy z morskej vody získava množstvo ďalších látok. Zvyčajne sú vedľajšími produktmi pri výrobe soli alebo sa získavajú prechodným sprostredkovaním určitých rastlín alebo rýb.
Prvýkrát objavil jód v popole rias v roku 1811 Francúz Bernard Courtois, majiteľ továrne na ľad. Pri hľadaní vhodnej suroviny na výrobu alkálií sa rozhodol použiť na tento účel riasy. Čistením reakčných nádob, ktoré obsahovali horúcu koncentrovanú kyselinu sírovú, upozornil na uvoľňovanie fialových výparov z popola rias. Na stenách chladnejšej časti nádoby kondenzovali pary vo forme tmavých kryštálov podobných kovu (Armstrong a Miall, 1946). Zistilo sa, že obsah jódu v niektorých riasach, najmä v Laminaria, je asi 0,5 % na suchom vzduchu. Koncentrácia jódu v morskej vode je približne 0,05 mg/l alebo približne 0,000005 %. V týchto typoch rias sa teda vyskytuje 100 000-násobok koncentrácie jódu v porovnaní s jeho obsahom v morskej vode.
Čoskoro po objavení Courtoisa sa zistil význam jódu pre medicínu. Najmä v severnom Anglicku sa začal intenzívny rozvoj priemyslu získavania jódu z morských rias. V roku 1846 bolo v Glasgowe viac ako 12 tovární na extrakciu jódu z morských rias. Objav jódu v čilských ložiskách dusičnanov však viedol k poklesu produkcie jódu z morských rias.
Približne v rovnakom čase sa z morských rias extrahovalo značné množstvo draselných a sodných solí. Technológia tohto procesu v podstate nebola vyvinutá. Zvyčajne sa uskutočňovalo jednoduché vylúhovanie rias vodou a následné odparenie vzniknutého roztoku. Ďalším veľmi rozšíreným spôsobom výroby solí bolo spálenie rias a vylúhovanie popola vodou. V dôsledku týchto primitívnych procesov sa jód získaval vo forme zlúčenín - jodidov draselných alebo sodných, ktoré sa po zmiešaní s kyselinou sírovou a oxidom manganičitým redukovali na elementárny jód.
V histórii používania rias existujú tri rôzne obdobia: a) prvé - keď sa riasy používali ako surovina na výrobu alkálií, b) druhé - keď sa používali na extrakciu jódu, a c) tretí - keď bol potaš extrahovaný z rias. Každé z období však skončilo vytvorením pokročilejších metód získavania týchto produktov z lacnejších surovín ťažených na súši. V súčasnosti sa riasy používajú ako surovina na výrobu alginátu sodného, organickej zlúčeniny používanej ako želatínotvorné a emulgačné činidlo pri výrobe potravín. Veľké podniky spracúvajúce morské riasy ako surovinu na výrobu predmetných chemických zlúčenín sa nachádzajú na pobreží južnej Kalifornie. V mnohých častiach sveta, najmä na východe, sú riasy široko používané ako potrava. V niektorých prímorských krajinách sa používajú ako hnojivá.
Extrakcia minerálnych zlúčenín počas odsoľovania morskej vody
V posledných rokoch sa osobitná pozornosť venuje problému odsoľovania morskej vody. Spravidla je koncentrácia solí v odpadových vodách v tomto prípade mnohonásobne vyššia ako obsah týchto solí v pôvodnej morskej vode. V priebehu prác na extrakcii minerálnych zlúčenín z takýchto soľaniek sa získali veľmi povzbudivé výsledky. Ide o zníženie nákladov na čerpanie vody vstupujúcej do spracovateľského závodu s relatívne vysokou teplotou soľanky a približne 4-krát vyššou koncentráciou.
Ak sa ukáže, že proces odsoľovania morskej vody je nákladovo efektívny, potom množstvo minerálnych zlúčenín, ktoré by bolo možné získať z odpadovej vody, bude mnohonásobne väčšie ako očakávaný dopyt. Predpokladajme napríklad, že v najbližších desaťročiach počet obyvateľov pobrežných regiónov dosiahne približne 100 miliónov ľudí, ktorí ročne spotrebujú v priemere 100 tisíc galónov vody na obyvateľa na domáce a priemyselné účely. Táto miera spotreby môže nakoniec dosiahnuť hodnotu približne 1013 galónov alebo 10 cu. míle vody ročne. Pri príjme tohto objemu vody z oceánu a účinnosti extrakcie sladkej vody 25%, 6,4 miliardy ton chloridu sodného, 240 miliónov ton horčíka, 160 miliónov ton síry, 800 tisíc ton bóru, 2 tisíc ton hliníka, 400 ton mangánu, 560 ton medi, 560 ton uránu, 2 tisíc ton molybdénu, 40 ton striebra a asi 1 tona zlata. Budeme predpokladať, že je ekonomicky výhodné vyťažiť len 10 % týchto množstiev a že obyvateľstvo, pre ktoré sa odsoľovanie morskej vody realizovalo, je schopné tieto minerálne zložky spotrebovať. Potom na základe štatistických údajov umiestnených v tabuľke. 3 môžeme konštatovať, že rýchlosti ťažby molybdénu, bóru a brómu budú zodpovedať ich spotrebe, pričom produkcia ostatných minerálnych zlúčenín bude výrazne prevyšovať dopyt po týchto látkach. Samozrejme, nie je potrebné extrahovať všetky soli. Odporúča sa získavať len tie soli, ktoré sú na trhu. V každom prípade je vzhľadom na technické ťažkosti nepravdepodobné, že by v súčasnosti prebiehala priemyselná ťažba akéhokoľvek prvku, ktorého koncentrácia v morskej vode je nižšia ako koncentrácia bóru. Nasledujúce úvahy si však zaslúžia pozornosť. Ak by bolo možné extrahovať urán a tórium z morskej vody, potom by použitie týchto prvkov v reaktoroch množiteľského typu zabezpečilo tepelnú energiu potrebnú na prevádzku konverzných závodov na výrobu sladkej vody.
| Element | Výročný produktov, t |
Produkcia na obyvateľa obyvateľov s obecnou jeho sila 108 osoba, t/rok |
Súčasné spotreba v USA na obyvateľa populácia, t/rok |
Postoj výroby na spotrebu |
| NaCl | 64*10 8 | 64 | 0,145 | 440 |
| magnézium | 2,4*10 8 | 2,4 | 25*10 -4 | 10000 |
| Síra | 1,6*10 8 | 1,6 | 0,033 | 50 |
| Draslík | 68*10 6 | 0,68 | 0,010 | 68 |
| bróm | 1,2*10 6 | 0,012 | 4,7*10 -4 | 25 |
| Bor | 0,8*10 6 | 0,008 | 5,5*10 -4 | 15 |
| hliník | 2000 | 2*10 -5 | 0,013 | 0,001 |
| mangán | 400 | 4*10 -6 | 0,0033 | 0,001 |
| Meď | 560 | 7*10 -6 | 0,0067 | 0,001 |
| Urán | 560 | 5*10 -6 | 1,4*10 -4 | 0,04 |
| molybdén | 2000 | 2*10 -5 | 8,3*10 -5 | 24 |
| Strieborná | 40 | 6*10 -7 | 3,0*10 -5 | 0,02 |
| Nikel | 400 | 4*10 -6 | 0,001 | 0,004 |
| Zlato | 1 | 2*10 -9 | 5,0*10 -6 | 0,0004 |
Teraz boli navrhnuté veľké jadrové reaktory, ktoré by mohli poskytovať tepelnú a elektrickú energiu pre konverzie odsoľovacích zariadení (Hammond, 1962) Odhaduje sa, že náklady na výrobu sladkej vody sú asi 0,15 USD na 1000 galónov, čo je v porovnaní s nákladmi na spotrebovanú vodu. v mestských oblastiach alebo na účely zavlažovania v niektorých oblastiach. Veľká reaktorová elektráreň môže denne vyprodukovať asi 109 galónov sladkej vody; toto množstvo by malo stačiť na pokrytie domácich a ekonomických potrieb mesta so 4 miliónmi obyvateľov alebo na zavlažovanie plodín s rozlohou 500 metrov štvorcových. míľ. Je však ťažké očakávať, že takéto rastliny sa v najbližších desaťročiach stanú vážnymi zdrojmi sladkej vody. Nedostatočne podložený je aj predpoklad o budúcej spotrebe minerálnych zložiek morskej vody a charaktere zmien cien a iných nákladov. Inými slovami, štatistické výpočty umiestnené v tabuľke. 3 majú iba teoretickú hodnotu.
N. V. Pertsov, 3. P. Ulberg, L. G. Iarochko, P. I. Gvoedyak, S 3 1 u4M lYa
"F Tumansky (7l) Žiadateľ
Ústav koloidnej chémie a chémie vody (5Y) METÓDA EXTRAKCIE ZLATA Z VODY
Vynález sa týka koloidnej chémie a možno ho použiť na čistenie vodných disperzií a odpadových vôd zo suspendovaných pevných látok, vrátane jemne rozptýleného zlata, v ťažobnom a klenotníckom priemysle a v iných podnikoch metalurgie neželezných kovov.
Známy je spôsob získavania zlata z horniny pomocou baktérií, ktorý spočíva v tom, že prenesú zlato do roztoku, z ktorého sa odstráni iónomeničovou metódou O).
Mikroorganizmy však extrahujú zlato obsiahnuté v častici horniny, pričom sa súčasne kultivujú na jej povrchu, v neprítomnosti tohto nevedie ich použitie na extrakciu napríklad koloidného zlata z roztoku k efektu. je nemožnosť použitia metódy pre veľmi zriedené roztoky. Metóda je tiež veľmi špecifická, zložitá a zdĺhavá.
Známy je aj spôsob úpravy odpadovej a pracej vody, ktorý spočíva v ich filtrácii cez iónomeničové kolóny, ktorý je založený na procese fixácie kovových iónov alebo zlúčenín kovov v iónovej forme, najčastejšie dinky, medi alebo drahších, napríklad zlato, častice ionit (2).
To však nezadrží vysoko rozptýlené kovové častice, vr. zlato, ktorého rozptyl je 200-300A. Pri prechode iónomeničom roztok obsahujúci zlato v iónovom stave s koncentráciou 0,03 r/ë (vo forme dikyanurátu) a koloidné zlato 0,03 g/l, zlato v iónovom stave zostáva menej ako 0,001 g/l, pričom obsah koloidného zlata sa mení o 10-12F. V umývaní
3 a odpadových vôd z klenotníckych tovární a iných odvetví zostáva až až
15 mg/l koloidného zlata, ktoré nie je možné odstrániť existujúcimi metódami. Technológia iónovej výmeny zabezpečuje potrebu regeneračného stupňa spojeného so spotrebou značného množstva solí, kyselín a zásad, ako aj hotového produktu – čistej vody. Percento extrakcie koloidného zlata je 10-143 a iónové
Cieľom vynálezu je zvýšiť stupeň extrakcie zlata z vody.
Tento cieľ sa dosahuje zavedením kvasiniek, rodov Saccharomyces alebo Candida do vody obsahujúcej zlato v koloidnom stave. alebo Rodotorula, alebo Escher i chia baktérie, zmes sa výhodne nechá 5 až 45 minút, dispergovaná fáza sa oddelí a zlato sa získa. Je výhodné zaviesť mikroorganizmy v množstve 106-10 buniek/ml na 1 mg/ml zlata.
Metóda sa vykonáva nasledujúcim spôsobom: 30
Používajú sa kultúry známej a používanej technológie mikroorganizmov - kvasinky Sa ccha romyces alebo Candida, alebo Rodotorula, príp.
Escherichia z 11.
Kvasinkové kultúry sa pestujú počas dňa na mladinovom agare a baktérie - na mäsovo-peptónovom agare, premytom fyziologickým roztokom (10 4 mol / l NaC
b" 8 na nefelometrovej kyvete FZK-56 3,055 a svetelný filter 6 sa zavedie do vodného roztoku zlata s koncentráciou 0,030,24 mg/ml, uchováva sa po dobu
5-45 min., potom sa dispergovaná fáza oddelí odstredením alebo elektroretenciou a zlato sa získa napríklad spálením výslednej hmoty. Obsah zlata je určený. UV spektrofotometer s použitím kalibračnej krivky.
Optimálny čas je odlišný pre rôzne typy mikroorganizmov, napríklad pre Saccharomyces vini u Candida ,util!s 15 min, Rodotorulà glutinis—
30 min a pre baktérie Escherichia
coli - 45 min, navyše schopnosť mikroorganizmov agregovať sa so zlatom závisí od veku kultúry ° Napríklad pri 4-dňovej kultúre sa potrebný kontaktný čas v porovnaní s 2-dňovou kultúrou zvyšuje.
Príklad 1. Do 50 ml odpadovej vody z klenotníctva s obsahom koloidného zlata o koncentrácii
0,03 mg/ml pridajte 50 ml suspenzie kultúry Saccharomyces vini s koncentráciou 3 ° 10 buniek/ml. Kontaktný čas 30 min. Výsledná hmota sa odstreďuje 5 minút pri
5000 ot./min., odlučovanie vody. Obsah zlata v druhom je
0,001 mg/ml. Zároveň extrahujú
1,40 kg zlata.
Príklad 2. Do 50 ml vodnej disperzie s obsahom 0,24 mg/ml koloidného zlata sa pridá 50 ml suspenzie kultúry Saccharomyces vlni s koncentráciou 3,108 buniek/ml Doba kontaktu je 45 minút. prešiel cez elektroretenčný článok, ktorý pozostáva z centrálnej pracovnej komory a dvoch elektródových komôr oddelených od pracovných celofánových membrán.
Centrálna komora článku je naplnená granulovaným silikagélom. V pracovnej komore vytvorte elektrické pole o sile 50 V/cm pri prietoku 1,5 ml/min. Podľa
UV spektrofotometer je kompletná extrakcia (retencia na silikagéli) dispergovaného zlata. V tabuľke sú uvedené porovnávacie údaje o stupni extrakcie zlata z vody navrhovanými a známymi metódami.
Metóda umožňuje extrahovať vysoko disperzné zlato takmer úplne (o 98-993) z vodných roztokov a odpadových vôd.
Použitie navrhovanej metódy iba na jednom šperkovom vlákne poskytne očakávaný ekonomický efekt 50-60 tisíc rubľov. za rok, 948897
S C5 a c5 b-o
I5 x bx o x
С1 asi do asi.
Stred cd cd o o o
° ° m m a s i
U o c () x c čo c
LA sch o o o o o
° ° o o a o
SL CA o o o bb \ SS \ o o o o o
Oh oh m oh oh
Zostavil G. Lebedeva
Editor M. Tovtin Tekhred M. Nagy Korektor G. Reshetnik
Objednávka 5688/1
Náklad 981 Podpísaný
VNIIPI Štátneho výboru ZSSR pre vynálezy a objavy
113035, Moskva, N-35, Raushskaya náb., 4/5 pobočka PPP "Patent", Užhorod, ul. Dizajn, 4
Prípravok podľa vynálezu sa zavádza do vody v množstve 1010 buniek/ml na 1 mg/ml zlata.
1. Spôsob získavania zlata z vody - 3. Spôsob podľa odstavcov. 1 a 2, z vrchnákov, vyznačujúci sa tým, že na zvýšenie stupňa extrakcie mikroorganizmami sa voda udržiava v prúdoch, najprv sa do vody privedie - my 5-45 min. kvasinky rodov Saccharomyces, alebo Can- Zdroje informácií, dida, alebo Rodotorula, alebo baktérie zohľadňované pri vyšetrení.
Už v roku 1903 bol navrhnutý amalgamačný proces a zariadenie na extrakciu zlata z morskej vody v kovovej forme.
Vopred prefiltrovaná morská voda sa pumpovala cez rúrku na dno kónickej lievikovitej nádoby s obsahom ortuti a delila sa perforovanými plechmi do mnohých sekcií (obr. 92). Po uvedení do kontaktu s ortuťou stúpajúci prúd vody prešiel cez sieťku na zachytenie jemnej pemzovej ortuti, potom cez perforované kontaktné fólie a nakoniec cez amalgamačný prepad umiestnený v hornej časti zariadenia a navrhnutý tak, aby úplne zachytil amalgamovanú ortuť. zlato z toku. Amalgám bol spracovaný konvenčnými metódami (stláčanie, stripovanie a tavenie).
Podobné zariadenie navrhol Ritter1 a líši sa tým, že jemná ortuť a zlato v nej obsiahnuté, ktoré obišli mriežku, sú zachytené vo vlnitom zariadení.
Iónová flotácia
Ako je uvedené vyššie (pozri kapitolu IV), iónová flotácia je založená na schopnosti niektorých heteropolárnych zlúčenín interagovať s iónmi ťažkých kovov, a najmä so zlatom, za vzniku plávajúcej nerozpustnej zlúčeniny. Najznámejšie diela v tomto smere sú tie, ktoré súvisia s morskou vodou Sebba (Južná Afrika) 189 J.
Sorpcia
Jedným z prvých sorbentov na extrakciu zlata z morskej vody boli testované uhlíkaté materiály. Takže na začiatku 20. storočia Parker zistil, že viskózne materiály obsahujúce uhlík, ako je asfalt, bitúmen, minerálny decht a iné, majú afinitu k voľnému zlatu. Na tomto základe Parker navrhol zachytávať jemne rozptýlené (alebo takzvané plávajúce) zlato z morskej vody jeho selektívnou fixáciou na pevné, viskózne lôžka obsahujúce uhlík uložené na tyčiach a pásoch inštalovaných v prúde. Zabezpečenie nepretržitého kontaktu sladkej vody s viskóznym materiálom sa musí vykonávať pôsobením prílivu a odlivu mora.
Väčšina výskumníkov sa však domnieva, že spomedzi sorbentov obsahujúcich uhlík je pre sorpciu zlata z morskej vody najzaujímavejšie aktívne uhlie.
Priekopníci tohto smeru, nemeckí výskumníci Nagel a Baur (1912-1913), navrhli použiť na sorpciu zlata z morskej vody koks, drevené uhlie a živočíšne uhlie a niektoré ďalšie adsorbenty. V experimentoch morská voda po predbežnom vyčírení pomocou pieskového filtra (na odstránenie suspendovaného materiálu a želatínových mikroorganizmov) prechádzala cez filtračné lôžko z koksu, uhlia alebo iného materiálu obsahujúceho uhlík pomocou metódy voľnej perkolácie alebo vzostupnej filtrácie (obr. 93). Obohatený adsorbent sa periodicky odstraňoval a pretavoval.
Na zníženie nákladov na čerpanie morskej vody sa navrhuje použiť na palube lode perforované nádoby s adsorbčným lôžkom, alebo pobrežné kade s falošným dnom a vrstvou adsorbentu pokrytou drôtenou alebo látkovou sieťkou, naplnené prílivovým účinkom.
Paralelne sa s použitím klasického adsorbentu (aktívne uhlie) uskutočnili štúdie s anorganickými sorbentmi s vysoko vyvinutým povrchom, ako sú čerstvo vyzrážané hydroxidy (hliník, železo, silikagél), koagulovaná hydrocelulóza a pod. navrhol použiť pobrežné kade alebo špeciálne tácky naplnené anorganickým sorbentom a úplne pokryté dvojitou vrstvou vláknitého textilného materiálu. Tácky sú ponorené do morskej vody na týždne a často aj mesiace, potom sa ošetria roztokmi kyanidu, aby sa extrahovalo adsorbované zlato. Pozlátené tácky sa používajú opakovane.
Pri štúdiu možných sorpčných metód sa zistilo, že pri tomto procese je výhodnejšie extrahovať kov koloidného zlata. Preto bolo prirodzené hľadať sorbent, ktorý by súčasne zredukoval halogénové zlato do kovového stavu a vytvoril čerstvo vytvorený aktívny povrch. Skúmaním širokého spektra takýchto možných sorbentov dospel Parker k záveru, že pre čo najkompletnejšiu extrakciu zlata z morskej vody je výhodný síran železnatý, ktorého optimálna spotreba je 2 kg/t vody.
Následne Parker získal samostatný patent2 na hardvérový dizajn adsorpčnej metódy s použitím siričitanu železnatého.
Kombinácia procesov redukcie halogenidu a adsorpcie koloidného zlata je pozorovaná aj v návrhoch iných výskumníkov. Bardt teda odporučil upraviť morskú vodu sulfitovým výluhom (odpadový produkt výroby celulózy) ako redukčným činidlom a následne ju zmiešať so zmesou jemne mletého uhlia a práškového kovu (napríklad medi, železa atď.) 3. Zrazenina obsahujúca ušľachtilé kovy sa najskôr spálila (na odstránenie uhlíka) a potom sa roztavila, aby sa zhromaždilo zlato v sprievodnom kove.
Podobný cieľ (získavanie halogenidového zlata a úplné zachytenie koloidného zlata) sledovali Glazunov a spolupracovníci (Paríž, 1928), ktorí navrhli použiť sulfidy, a najmä pyrity, ako adsorbent pre zlato rozpustené v morskej vode.
Túto myšlienku prakticky zrealizovali až v roku 1953 Walthers a Stillman, ktorí sa vydali vlastnou originálnou cestou. Podľa ich návrhu bola sulfidická ruda nahromadená za betónovou stenou postavenou v blízkosti spodnej línie prílivu a zakrivenou smerom k brehu. Pri prílive bola ruda zaplavená vodou a pri odlive voda presakovala cez rudu. Tento cyklus sa mnohokrát opakoval. Po určitom čase sa suspenzia rozložených sulfidov obsahujúcich adsorbované zlato pri odlive odstránila a roztopila. Vynálezcovia poznamenali, že zrážanie zlata sulfidmi je uľahčené vystavením morskej vody rádioaktívnym prvkom.
Neskôr Stokes ukázal, že na vyzrážanie zlata z morskej vody sa dá použiť široká škála prírodných a umelých sulfidových materiálov, pričom sulfid antimonitý je veľmi účinný.
Na zintenzívnenie procesu sorpcie zlata sulfidmi pri súčasnom eliminovaní nákladov na čerpanie morskej vody Gernick a Stokes navrhli špeciálny prístroj d, v literatúre nazývaný „lapač sulfidu antimónu“ (keďže bol koncipovaný na použitie ako adsorbent, sulfid antimónový) alebo „systém prílivovej energie“. Toto zariadenie je vyrobené vo forme rúrky v tvare obráteného U, ktorej jedno koleno je vybavené predĺžením, v ktorom je medzi mriežky umiestnený adsorbent (aktívne uhlie alebo sulfidy). Touto trubicou preteká morská voda pod vplyvom prílivového prúdu alebo pri pohybe plavidla, ku ktorému je pripojený popísaný prístroj.
Za posledných 10-15 rokov sa objavilo množstvo patentov, ktoré zlepšujú sorpčnú extrakciu zlata z morskej vody pomocou sulfidov kovov 2. Najoriginálnejší nápad a vybavenie v tomto smere predstavil americký výskumník Norris 3.
Jeho najnovší vynález je založený na použití čerstvo nanesených koloidov sulfidov kovov adsorbovaných na povrchu silných organických, syntetických alebo prírodných vlákien. Typickým príkladom syntetizovaných organických vlákien sú polymerizované akrylonitrilové alebo vinylkyanidové vlákna. Z prírodných vlákien je najvhodnejšia vláknina Ramie (čínska žihľava). Takéto vlákna, keď sa ponoria do riedkej koloidnej suspenzie (napríklad čerstvo vyzrážaný sulfid zinočnatý, pripravený zmiešaním zriedených roztokov chloridu zinočnatého a sulfidu sodného pri hodnote pH približne 6,0), budú aktívne adsorbovať významnú časť častíc koloidného sulfidu. a pevne držia na ich povrchu. .
Pri kontakte takto pripravených sorpčných vlákien s chudobnými roztokmi obsahujúcimi zlato (napríklad morskou vodou) sa adsorbujú ióny ušľachtilých kovov. Z vlákien ich možno odstrániť úpravou zohriatymi zriedenými roztokmi kyanidu sodného s malým prídavkom peroxidu vodíka alebo chlórnanom sodným s malým prídavkom kyseliny chlorovodíkovej. Potom, čo boli adsorbované ióny eluované, môžu sa vlákna po predbežnej úprave suspenziou sulfidu zinočnatého niekoľkokrát premyť a znovu použiť. Okrem sulfidu zinočnatého sa v tomto procese môžu použiť sulfidy železa, mangánu, medi, niklu a olova.
Dlhodobé štúdie Norrisa preukázali, že určité oxidačné plyny, ktoré sú často rozpustené vo väčšine morských vôd, môžu nepriaznivo ovplyvniť použité kolektory a adsorpčné vlákna. Tieto plyny zahŕňajú kyslík, dusík a oxid uhličitý. Preto, aby sa dosiahol čo najväčší účinok, navrhované zariadenie musí mať prostriedky na nepretržité odstraňovanie takýchto plynov z prúdiacej morskej vody predtým, ako sa dostane do kontaktu so zbernou štruktúrou vlákien.Navyše vzhľadom na relatívne malý počet kovových iónov, ktoré sa zhromažďujú v jednej bežnej operácii, rovnako ako zložitosť spracovania a manipulácie s vláknitou hmotou, je žiaduce vykonávať všetky operácie nepretržite a automaticky. Všetky tieto faktory boli zohľadnené v prístroji navrhnutom Norrisom (obr. 94).
Pre výskumníkov je obzvlášť zaujímavé používanie prírodných a umelých iónomeničov na extrakciu zlata a striebra z morskej vody.
Prioritu v tomto smere má Brook, ktorý v roku 1953 navrhol použiť na extrakciu striebra z morskej vody zeolity železa a mangánu.
Neskôr, v roku 1964, Bayer a spolupracovníci (Nemecko) vytvorili takzvané chelátové iónomeničové živice schopné extrahovať až 100 % cenných kovov z morskej vody.
Z najnovších prác venovaných využitiu pevných iónomeničov na extrakciu zlata z morskej vody je najzaujímavejšia štúdia skupiny experimentátorov z Gouffa Research and Development Company (USA).
Na zber ušľachtilých kovov sa navrhuje použiť vo vode nerozpustný etylénový polymér obsahujúci visiace karboxylátové alebo amidové skupiny. Jedným z najlepších spôsobov získania tohto polyméru je zmydelnenie etylénalkylakrylátového kopolyméru alebo syntéza kopolyméru etylénu a esteru kyslých skupín vrátane kyseliny maleínovej, fumárovej a takónovej. Príprava takýchto sorbentov je podrobne opísaná v patente.
Po dosiahnutí dostatočného stupňa naplnenia polymérneho filmu je možné adsorbované zlato extrahovať roztavením z popola po spálení polyméru alebo vyzrážať z roztokov z rozpustenia polymérov v hydroxide sodnom (kaustic soda).
Spôsoby použitia prírodných a umelých iónomeničov sú v zásade rovnaké ako u vyššie diskutovaných sorbentov, a to: inštalácia do prúdu morskej vody, filtrácia cez lôžko vo vani, nakladanie poréznych nádob.
Murro navrhol úplne nový spôsob využitia umelých iónových výmenníkov – ich aplikovanie na trup lode na komerčnú plavbu. Po príchode do prístavu určenia možno iónomeničovú živicu z lode odstrániť a spracovať. Úprava živicou spočíva v premývaní kyselinami a špeciálnymi prvkami, po ktorej nasleduje elektrolýza eluátu s obsahom drahých kovov. Regenerované živice je možné použiť opakovane.
Najekonomickejším návrhom je použitie špeciálnych zariadení umiestnených v nákladnom priestore nádoby a naplnených iónomeničovými živicami. Tu sa predpokladá, že pohyb lode vpred spôsobí, že morská voda nepretržite prúdi cez nádobu s iónomeničom. Táto nádoba by mala mať plochu prierezu asi 9,5-10 m2, dĺžku 3 ma obsahovať asi 28 m3 živice. Maximálny prietok morskej vody pri sorbovaní na živicu by mal byť -0,8 m3 až 1 m2 povrchu za minútu (0,8 m/min).
Pri takomto prietoku prejde cez sorpčné zariadenie -12 500 ton morskej vody za deň. Pri držaní vo vode dokonca
1 mg!t zlata denne vyťaží 12,5 g zlata. Počas roka nepretržitého plávania sa môže adsorbovať asi 4,5 kg zlata v hodnote asi 5 000 dolárov.
Cementácia
Jedna z mála správ o praktickej aplikácii metódy cementovania zlata z morskej vody sa týka americkej patentovanej Parkerovej metódy. Ako tmeliaci kov sa navrhuje niklový prach. Redukciou, substitúciou a adsorpciou možno z morskej vody izolovať zlato, prítomné v halogénovej aj elementárnej forme.
Pri nauhličovaní zmiešaním niklového prášku s morskou vodou je možné dosiahnuť jeho obsah zlata od 15 do 20 % hmotnosti. Naplnený niklový prášok sa vyberie z kade a roztaví sa.
Na vyzrážanie zlata z veľmi chudobných morských vôd Sneming navrhol použiť zvýšenú afinitu zlata k telúru. Zistilo sa, že je najvýhodnejšie uskutočňovať nanášanie s amorfným telúrom s vysoko vyvinutým reakčným povrchom. Takéto tmeliace činidlo sa získa spracovaním rozpustnej soli telúru s oxidom siričitým. Morská voda je filtrovaná cez pevnú vrstvu amorfného telúru. Na extrakciu vyzrážaného zlata sa obohatená hmota zahreje na sublimáciu telúru (s jeho následným zachytením) a zvyšok sa roztaví na zlato.